El diagrama de Lewis (o regla de octeto) se usa para determinar cuántos electrones de valencia están presentes en un átomo (la menor unidad existente de materia), pues a través de ellos se hacen los enlaces que les dan forma a las moléculas.
Se trata de un método creado en el año 1916 por el fisicoquímico de origen estadounidense, Gilbert Newton Lewis, en uno de sus más famosos trabajos, denominado “La molécula y el átomo”.
Realmente se basa en una estructura sumamente sencilla, no obstante, es imprescindible conocer algunos conceptos básicos sobre química, para comprender mejor.
Por eso aclararemos qué es el diagrama de Lewis, cuál es la regla adecuada para aprender cómo hacerlo, y mencionaremos varios ejemplos relacionados con este tema.
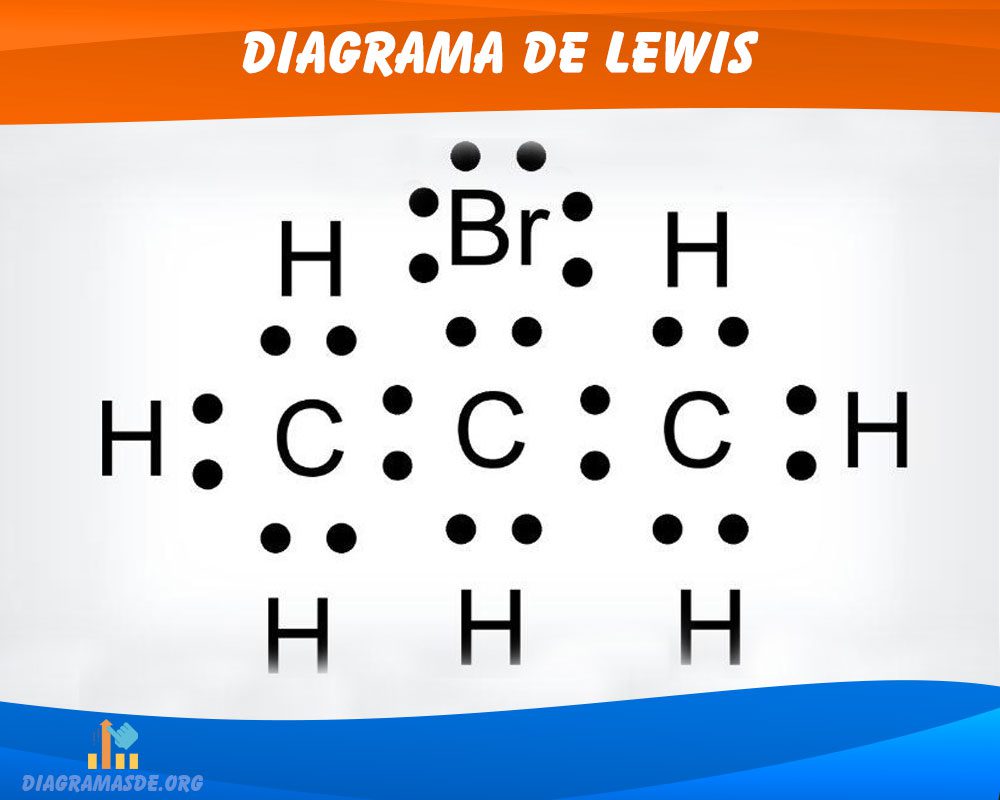
Dato curioso, este es uno de los diagramas que más nombres recibe, también se lo conoce como
- diagrama de punto y raya diagonal
- modelo de Lewis
- diagrama de valencia
- regla de octeto
Tabla de Contenidos
Qué es el diagrama o estructura de Lewis?
A este método también se le conoce como “estructura de Lewis”, y es una representación gráfica a través de la cual se muestran todos los electrones que lleva un átomo en su capa exterior, aquellos capaces de mezclarse con otros, es decir, los de “valencia”.
Por lo tanto, esta fórmula sirve de modelo para explicar la manera en la que los átomos pueden construir enlaces químicos entre sí, mediante el emparejamiento de sus electrones de valencia.
Estos son realmente partículas subatómicas con cargas eléctricas negativas (e-) que, junto a los protones (partículas subatómicas de carga positiva “e+”) y los neutrones (de carga neutral), constituyen a los átomos.
En este sentido, cada átomo está compuesto por un núcleo, neutrones, protones y electrones. Estos últimos son los encargados de conectarse con las demás partículas negativas de otros átomos, para unirlos y darle vida a las moléculas.
De allí que Lewis ideara la ingeniosa regla de los octetos, una fórmula eficaz para simplificar este impresionante fenómeno químico.
Regla del octeto: ¿por qué es esencial para la estructura de Lewis?
La regla del octeto también es una teoría planteada por Lewis en el año 1916, y se basa en una norma simple: los elementos se logran estabilizar cuando la última capa de electrones en cada uno de sus átomos, acumula 8 partículas de valencia.
Esto ocurre porque los átomos cuya capa exterior carece del número adecuado de partículas con carga negativa, tratan de enlazarse a otras unidades mínimas de materia para poder completar dicha cantidad de electrones.
Para entenderlo mejor es necesario saber que los átomos cuentan con una cifra exacta tanto de protones, como de electrones, pero los primeros se mantienen dentro del núcleo junto a los neutrones, mientras el resto, los de carga “e-”, se van distribuyendo por capas y orbitan alrededor del centro atómico.
Esa es la razón de que la mayoría de los átomos, por sí solos, no posean 8 electrones en su capa de valencia, por ello, esas partículas de carga negativa inician el proceso de atracción para compensar la ausencia y estabilizarse.
A esa unión en la que se comparten electrones para formar moléculas se le llama “enlace covalente”, y al conseguir la estabilidad a través de dicho intercambio químico, los elementos se identifican dentro de la categoría conocida como “gases nobles”.
¿Cómo hacer el diagrama de Lewis?
Para realizar el diagrama de Lewis debemos tomar como referencia principal la regla del octeto, pero también tenemos que considerar otros aspectos importantes.
Por ejemplo, los electrones de valencia se unen en pares; los elementos o átomos se identifican con una simbología específica (“H” para hidrógeno, “CL” en el caso de cloro, etc); los enlaces covalentes se distinguen con una línea por cada par de electrones; pero los electrones solitarios, es decir, aquellos que no se comparten entre dos o más átomos, se representan con puntos y asteriscos.
Ahora bien, tomando todos estos datos en cuenta, podemos iniciar el proceso para elaborar la estructura de Lewis siguiendo los pasos que mencionaremos a continuación:
- Dibuja el esqueleto molecular: coloca el átomo con una menor cantidad de electrones de valencia, en el centro, y los demás elementos alrededor de él utilizando la fórmula correspondiente.
- Distribuye los electrones de valencia: utiliza puntos o asteriscos para los pares solitarios y líneas en el caso de los enlaces covalentes, de modo que se complete la regla del octeto en cada uno de los átomos.
- Identifica los enlaces covalentes: usa una línea si es una combinación simple entre dos electrones; dos rayas paralelas cuando se conecten dos pares de ellos; y tres líneas en los triples enlaces de pares.
Ejemplos de diagrama de Lewis
Veamos algunos ejemplos para despejar dudas en caso de hacer diagramas de Lewis con enlaces simples, dobles o triples:
Estructura molécula de Agua H2O
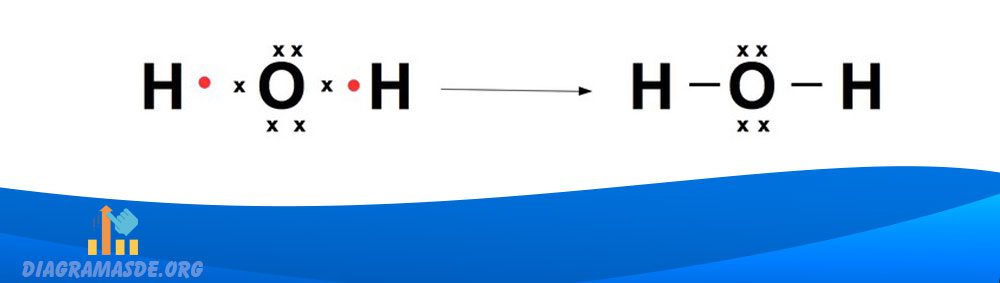
Estructura molécula Dióxido de Carbono CO2
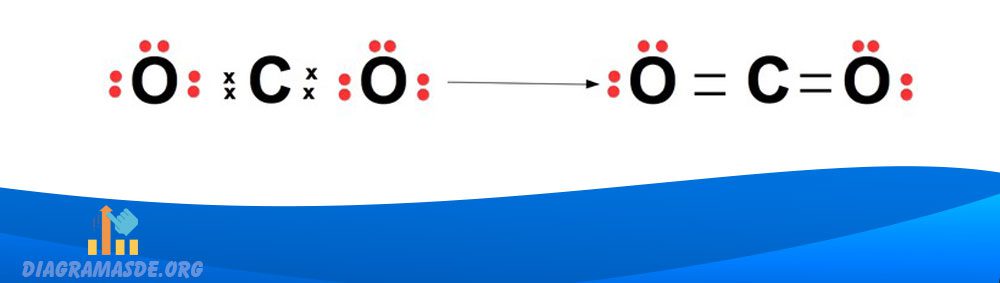
Estructura de Nitrógeno molecular N2:

Ejercicio reales para practicar
Ahora es tiempo de poner en práctica todos los conocimientos descritos a lo largo de este post, así que dejaremos varios ejercicios para finalizar:
- Dibuja el diagrama de Lewis del metano (CH4), y añade los enlaces covalentes considerando que el carburo (C) tiene 4 electrones de valencia, mientras el hidrógeno (H) posee 1:
- Dibuja el diagrama de Lewis del ioduro de estaño (SnI4), y añade los enlaces covalentes considerando que el estaño (Sn) tiene 4 electrones de valencia, mientras el iodo posee 7:
- Dibuja el diagrama de Lewis del sulfuro de potasio (K2S), y añade los enlaces covalentes considerando que el potasio (K) tiene 1 electrón de valencia, mientras el azufre (S) tiene 6: